今日の入試問題から 共有結合性物質の酸化数 [CVX-化学発展演習 日記]
こんにちは~ (*^_^*)/
今日は雨が強くて、めっぽう寒かったですね![[雨]](https://blog.ss-blog.jp/_images_e/3.gif)
今回は、こんな問題です。
「濃い亜硫酸ナトリウム水溶液に硫黄を加えて加熱した溶液を冷却すると、チオ硫酸ナトリウム五水和物 の無色透明な結晶が得られる。
Na2SO3 + S → Na2S2O3
この結晶は写真フィルムの定着工程に用いられる。これは未感光のハロゲン化銀にS2O3^2-が作用し、 銀の錯イオンとして溶かし出す作用を利用したものである。
AlCl + 2Na2S2O3 → Na3[Ag(S2O3)2] + NaCl
Na3[Ag(S2O3)2]における硫黄原子の酸化数はいくつか?」
というものですが、如何ですか?
化合物や多原子イオン(複数の原子からなるイオン)の酸化数は、優先順位に従って、付けていきます。
優先順位が高いのは、まず
アルカリ金属(+1),2族元素(+2),アルミニウム(+3),フッ素(-1) ですね。
次いで、
水素 +1
そして、
酸素 -2
の順です。
例えば、BaO2 と PbO2 の酸化数を考えた時、優先順位からバリウムBaは2族元素なので「+2」、鉛Pbは14族元素なので「+4」だと分かります。
よって、BaO2の酸素原子の酸化数は「-1」となり、BaO2は過酸化物であることが分かります。
さて、それでは、酢酸CH3-COOHは如何でしょう?
分子式はC2H4O2となり、炭素の酸化数が「0」となります。
しかし、これは間違い![[爆弾]](https://blog.ss-blog.jp/_images_e/154.gif)
共有結合では、共有結合している2つの原子のウチ、電気陰性度の大きい原子の方に共有電子対が全て奪われたと考えて酸化数を計算します。
電気陰性度は、水素H(2.1),炭素C(2.5),硫黄S(2.5),窒素N(3.0),酸素(3.5),フッ素(4.0)のようになっています(ポーリングの値)が、
例えば、
C-H であれば Cの酸化数は「-1」,Hの酸化数は「+1」
C=O であれば Cの酸化数は「+2」,Oの酸化数は「-2」 となります。
共有結合の価標1本あたり「±1」と覚えておくと良いでしょう。
ですから、シアン化水素HCNのそれぞれの原子の酸化数は、
H-C≡N なので Hが「+1」,Nが「-3」,Cは「-1」と「+3」の合計の「+2」です。
ちなみに、
配位結合は、電子供与体(ドナー)が共有電子対を一方的に電子受容体(アクセプター)へ貸し与える結合なので、ドナーの電気陰性度が大きい時は互いに「0」,小さい時には「±2」となります。
例えば、
N→Ag では NもAgも酸化数は「0」 ですが
S→O では Sは「+2」でOは「-2」 になります。
ですから、テトラアンミン銅(Ⅱ)イオンの場合、Nの酸化数はアンモニアNH3の時と同じ「-3」のままで、銅(Ⅱ)イオンの酸化数も単原子イオンの場合と同じ「+2」のままです。
さて、本題ですが、
チオ硫酸イオンは、硫酸イオンSO4^2-の酸素原子の1つが硫黄原子と置換した形をしています。
ですから、中心の硫黄原子と端っこの硫黄原子の酸化数は異なります。
中心の硫黄は下図の通り酸素Oにだけ配位結合しているので、酸化数は合計で「+5」になります。
端っこの硫黄の酸化数は「-1」です。
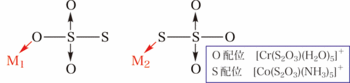
平均を取れば「+2」となりますが、単に「硫黄原子の酸化数」と問われれば、「-1と+5」と答えるべきでしょう。平均を尋ねられたのであれば「+2」と答えれば良いです。
計算問題では合計の酸化数で考えた方が早いですね。
酸化数の計算は、東京医科歯科大学でも「ビタミンC」の炭素の酸化数を求める問題が出題されていました。
共有結合や配位結合における酸化数についても、しっかりと学習しておきましょう。
今日は雨が強くて、めっぽう寒かったですね
今回は、こんな問題です。
「濃い亜硫酸ナトリウム水溶液に硫黄を加えて加熱した溶液を冷却すると、チオ硫酸ナトリウム五水和物 の無色透明な結晶が得られる。
Na2SO3 + S → Na2S2O3
この結晶は写真フィルムの定着工程に用いられる。これは未感光のハロゲン化銀にS2O3^2-が作用し、 銀の錯イオンとして溶かし出す作用を利用したものである。
AlCl + 2Na2S2O3 → Na3[Ag(S2O3)2] + NaCl
Na3[Ag(S2O3)2]における硫黄原子の酸化数はいくつか?」
というものですが、如何ですか?
化合物や多原子イオン(複数の原子からなるイオン)の酸化数は、優先順位に従って、付けていきます。
優先順位が高いのは、まず
アルカリ金属(+1),2族元素(+2),アルミニウム(+3),フッ素(-1) ですね。
次いで、
水素 +1
そして、
酸素 -2
の順です。
例えば、BaO2 と PbO2 の酸化数を考えた時、優先順位からバリウムBaは2族元素なので「+2」、鉛Pbは14族元素なので「+4」だと分かります。
よって、BaO2の酸素原子の酸化数は「-1」となり、BaO2は過酸化物であることが分かります。
さて、それでは、酢酸CH3-COOHは如何でしょう?
分子式はC2H4O2となり、炭素の酸化数が「0」となります。
しかし、これは間違い
共有結合では、共有結合している2つの原子のウチ、電気陰性度の大きい原子の方に共有電子対が全て奪われたと考えて酸化数を計算します。
電気陰性度は、水素H(2.1),炭素C(2.5),硫黄S(2.5),窒素N(3.0),酸素(3.5),フッ素(4.0)のようになっています(ポーリングの値)が、
例えば、
C-H であれば Cの酸化数は「-1」,Hの酸化数は「+1」
C=O であれば Cの酸化数は「+2」,Oの酸化数は「-2」 となります。
共有結合の価標1本あたり「±1」と覚えておくと良いでしょう。
ですから、シアン化水素HCNのそれぞれの原子の酸化数は、
H-C≡N なので Hが「+1」,Nが「-3」,Cは「-1」と「+3」の合計の「+2」です。
ちなみに、
配位結合は、電子供与体(ドナー)が共有電子対を一方的に電子受容体(アクセプター)へ貸し与える結合なので、ドナーの電気陰性度が大きい時は互いに「0」,小さい時には「±2」となります。
例えば、
N→Ag では NもAgも酸化数は「0」 ですが
S→O では Sは「+2」でOは「-2」 になります。
ですから、テトラアンミン銅(Ⅱ)イオンの場合、Nの酸化数はアンモニアNH3の時と同じ「-3」のままで、銅(Ⅱ)イオンの酸化数も単原子イオンの場合と同じ「+2」のままです。
さて、本題ですが、
チオ硫酸イオンは、硫酸イオンSO4^2-の酸素原子の1つが硫黄原子と置換した形をしています。
ですから、中心の硫黄原子と端っこの硫黄原子の酸化数は異なります。
中心の硫黄は下図の通り酸素Oにだけ配位結合しているので、酸化数は合計で「+5」になります。
端っこの硫黄の酸化数は「-1」です。

平均を取れば「+2」となりますが、単に「硫黄原子の酸化数」と問われれば、「-1と+5」と答えるべきでしょう。平均を尋ねられたのであれば「+2」と答えれば良いです。
計算問題では合計の酸化数で考えた方が早いですね。
酸化数の計算は、東京医科歯科大学でも「ビタミンC」の炭素の酸化数を求める問題が出題されていました。
共有結合や配位結合における酸化数についても、しっかりと学習しておきましょう。





コメント 0