春期講習 演習3-3 シクロアルカンの歪みエネルギー [C3J-東大化学 日記]
こんにちは~ (*^_^*)/
本日は、強風で電車![[電車]](https://blog.ss-blog.jp/_images_e/30.gif) は止まる,雨は降る
は止まる,雨は降る![[雨]](https://blog.ss-blog.jp/_images_e/3.gif)
![[バッド(下向き矢印)]](https://blog.ss-blog.jp/_images_e/156.gif) ・・・・で
・・・・で![[がく~(落胆した顔)]](https://blog.ss-blog.jp/_images_e/142.gif)
今回は、春期テキストの補完です。
C3Jテキスト(p55)の演習3-3(大阪市立大)の問2,4の比較です。
問2 下記の燃焼熱(kJ/mol)から、プロペンとシクロプロパンの生成熱を求める。
H2(気) C(黒鉛) プロペン(気) シクロプロパン(気)
286 394 2058 2091
問4 下記の結合エネルギー(kJ/mol)と黒鉛の昇華熱717(kJ/mol)から、プロペンと
シクロプロパンの生成熱を求める。
H-H C-H C-C C=C
(CH4) (アルカンの平均) (アルケンの平均)
436 416 348 612
※ (25℃,1013hPa)
の2問について考えてみよう。
問2は、ヘスの総熱量普遍の法則(熱力学第一法則と同じ→上級者向けの詳説)から、
プロペンの生成熱 -18kJ/mol
シクロプロパンの生成熱 -51kJ/mol
と求められます。
問4は、結合エネルギーの計算を使って、
プロペンの生成熱 -3kJ/mol
シクロプロパンの生成熱 +81kJ/mol
と求められます。
ここで、問2と問4の結果を見比べてみると、
プロペン(プロピレン)CH3-CH=CH2 の生成熱は、
-18 と-3 で計算方法による若干の誤差が生じていますが、極端な違いは見られませんね。
ところが、
環状アルカンのシクロプロパンの生成熱は、
燃焼熱からの計算では-51kJ/molとなるのに、結合エネルギーから求めた生成熱は+81kJ/molとなってしまいます。
東大なら、「この差が生じる理由を2行で説明せよ」との設問があるでしょうね。
ご存じの通り、鎖式飽和炭化水素における炭素はsp3混成しており、正四面体構造でC-C-Cの結合角は109.27°です。
このCの正四面体構造は安定で、特にメタンCH4は、湖沼などで有機物が微生物(メタン菌など)によって分解された最終生成物として排泄される程です。
しかしながら、環状アルカンのシクロプロパンのC-C-C結合角は60°と著しく歪んでおり、きわめて不安定な状態にあります。
そのため、シクロプロパンは、ニッケル触媒で水素を作用させると、簡単に三員環が開裂して水素が付加し安定なプロパンになります。ちなみにシクロブタンも水素付加で開裂してブタンになります(北海道大学の炭化水素C5H10の構造決定問題でその応用が出題)。
シクロヘキサンは、安定ないす型構造の時、歪みがほとんどありません。
下図は、その歪みによるエネルギーをまとめたものです。
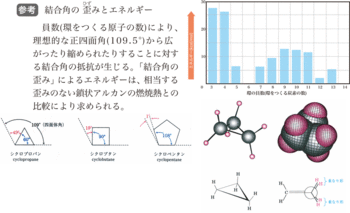
これを見れば、「問4の結合エネルギーの計算では、安定なアルカンAlkaneのC-C結合エネルギーで計算した為、歪みによるエネルギーが含まれていない」ということが分かりますね。
本日は、強風で電車
今回は、春期テキストの補完です。
C3Jテキスト(p55)の演習3-3(大阪市立大)の問2,4の比較です。
問2 下記の燃焼熱(kJ/mol)から、プロペンとシクロプロパンの生成熱を求める。
H2(気) C(黒鉛) プロペン(気) シクロプロパン(気)
286 394 2058 2091
問4 下記の結合エネルギー(kJ/mol)と黒鉛の昇華熱717(kJ/mol)から、プロペンと
シクロプロパンの生成熱を求める。
H-H C-H C-C C=C
(CH4) (アルカンの平均) (アルケンの平均)
436 416 348 612
※ (25℃,1013hPa)
の2問について考えてみよう。
問2は、ヘスの総熱量普遍の法則(熱力学第一法則と同じ→上級者向けの詳説)から、
プロペンの生成熱 -18kJ/mol
シクロプロパンの生成熱 -51kJ/mol
と求められます。
問4は、結合エネルギーの計算を使って、
プロペンの生成熱 -3kJ/mol
シクロプロパンの生成熱 +81kJ/mol
と求められます。
ここで、問2と問4の結果を見比べてみると、
プロペン(プロピレン)CH3-CH=CH2 の生成熱は、
-18 と-3 で計算方法による若干の誤差が生じていますが、極端な違いは見られませんね。
ところが、
環状アルカンのシクロプロパンの生成熱は、
燃焼熱からの計算では-51kJ/molとなるのに、結合エネルギーから求めた生成熱は+81kJ/molとなってしまいます。
東大なら、「この差が生じる理由を2行で説明せよ」との設問があるでしょうね。
ご存じの通り、鎖式飽和炭化水素における炭素はsp3混成しており、正四面体構造でC-C-Cの結合角は109.27°です。
このCの正四面体構造は安定で、特にメタンCH4は、湖沼などで有機物が微生物(メタン菌など)によって分解された最終生成物として排泄される程です。
しかしながら、環状アルカンのシクロプロパンのC-C-C結合角は60°と著しく歪んでおり、きわめて不安定な状態にあります。
そのため、シクロプロパンは、ニッケル触媒で水素を作用させると、簡単に三員環が開裂して水素が付加し安定なプロパンになります。ちなみにシクロブタンも水素付加で開裂してブタンになります(北海道大学の炭化水素C5H10の構造決定問題でその応用が出題)。
シクロヘキサンは、安定ないす型構造の時、歪みがほとんどありません。
下図は、その歪みによるエネルギーをまとめたものです。

これを見れば、「問4の結合エネルギーの計算では、安定なアルカンAlkaneのC-C結合エネルギーで計算した為、歪みによるエネルギーが含まれていない」ということが分かりますね。
春期講習 添削課題3 問4 安定な鉄鉱石 [C3J-東大化学 日記]
こんにちは~ (*^_^*)/
暖かくなってきましたね。
さて、今回は添削課題3の「酸化鉄の生成熱から鉄鉱石の成分を推定する問題」です。
設問の概略は、
「地球上の鉄は(中略)長い年月の間に、そのほとんどが酸化物に変化して埋蔵されているとする。FeOの生成熱267kJ/mol,Fe2O3の生成熱824kJ/mol,Fe3O4の生成熱1118kJ/molとすると、冷えて鉄鉱石に埋蔵されている酸化物は何か?」という内容でした。
「生成熱が大きい」=「生成物質のエンタルピー(熱含量)が小さい」=「熱化学的に安定な生成物」
に気がつけば簡単な問題ですが、提出された答案で意外と多かったのは、
「生成熱が最も大きいFe3O4」との解答でした。
生成物質1molに含まれる鉄Fe原子の数が異なるので、生成物質の安定性を比較する為には、Fe1molあたりの生成熱を比較する必要があります。
Fe1molあたり
FeOの生成熱は、267kJ
Fe2O3の生成熱は、824÷2=412kJ
Fe3O4の生成熱は、1118÷3≒373kJ
となるので、Fe2O3が最も安定と言う事になります。
鉄鉱石としては、赤鉄鉱や磁鉄鉱等が製鉄の原料として使われています。
暖かくなってきましたね。
さて、今回は添削課題3の「酸化鉄の生成熱から鉄鉱石の成分を推定する問題」です。
設問の概略は、
「地球上の鉄は(中略)長い年月の間に、そのほとんどが酸化物に変化して埋蔵されているとする。FeOの生成熱267kJ/mol,Fe2O3の生成熱824kJ/mol,Fe3O4の生成熱1118kJ/molとすると、冷えて鉄鉱石に埋蔵されている酸化物は何か?」という内容でした。
「生成熱が大きい」=「生成物質のエンタルピー(熱含量)が小さい」=「熱化学的に安定な生成物」
に気がつけば簡単な問題ですが、提出された答案で意外と多かったのは、
「生成熱が最も大きいFe3O4」との解答でした。
生成物質1molに含まれる鉄Fe原子の数が異なるので、生成物質の安定性を比較する為には、Fe1molあたりの生成熱を比較する必要があります。
Fe1molあたり
FeOの生成熱は、267kJ
Fe2O3の生成熱は、824÷2=412kJ
Fe3O4の生成熱は、1118÷3≒373kJ
となるので、Fe2O3が最も安定と言う事になります。
鉄鉱石としては、赤鉄鉱や磁鉄鉱等が製鉄の原料として使われています。
春期講習 添削課題4 (c) pHジャンプと指示薬 [C3J-東大化学 日記]
こんにちは~ (*^_^*)/
個人的には春期講習も一段落して一息・・・・というところですか。
先日までの寒の戻りから一転して、昨日は暖かい一日でした。
さて、
「知は力なり(Ipsa scientia potestas est)」となりと言いますが、まさに記述問題では知識の差が如実に得点差として表れます。
C3J添削課題4の問題(c)
「塩酸をNaOHで中和滴定した時に使用するpH指示薬」と
「酢酸をNaOHで滴定した時に使用するpH指示薬」の選定に関する記述
では、指示薬の変色域とpHジャンプ(pH飛躍)の関係がポイントになります。
指示薬(HInで表す)自身も、弱い酸または塩基で、
(酸性の色)HIn ⇄ H+ + In-(アルカリ性の色)
の平衡が存在し、色の変化が肉眼で認められる範囲は指示薬の色調によって異なりますが、
おおよそ 10 > (酸性色の濃さ)÷(アルカリ性色の濃さ) > 0.1 とされ、
酸型とアルカリ型を示すpHの間隔はおよそ2となります。
その間では、酸性型とアルカリ性型の濃度の比に応じた中間色を示します。
この中間色の範囲が変色域で、その中心はpKHInです。
pHが1の強酸10mLをpH13の強塩基で滴定した場合、
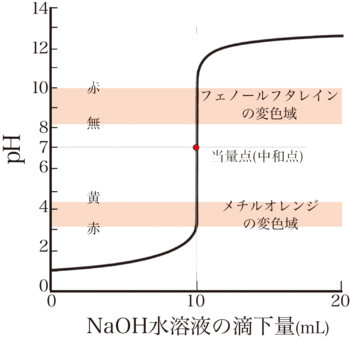
のような滴定曲線となります。
この滴定曲線の中で、中和点の前後で急激にpHが変化している部分がpHジャンプ(pH飛躍)です。pH指示薬は、その変色域がpH飛躍(pHジャンプ)の範囲内にあるものを選択する必要があります。
pHジャンプ(pH飛躍)が起こる理由は、
pH(水素イオン指数)が対数だからです。
下図に明らかなように、当量点に近づくほど、単位滴下量あたりのpHの変化が大きくなります。
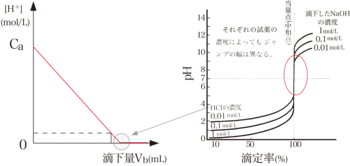
0.10mol/Lの塩酸10mLを0.10mol/LのNaOH水溶液で中和滴定すると、約8.2mL滴下したところで濃度が10分の1の0.010mol/Lになりますが、その10分の1の0.001mol/Lにするには1.6mLの滴下でよく、さらにその10分の1にするには0.18mLの追加で済みます。
このように、pHが1変化するのに要するNaOH水溶液の滴下量は、当量点(中和点)に近づくほど小さくなるため、滴定曲線の傾きは中和点でほぼ垂直(無限大)になるのです。
定量分析の実験手順と注意点,操作の意味は、
図解とフローチャートによる定量分析(技報堂出版) にフローチャート付きで詳しく記載されています。東大で頻出の実験に関する記述対策として、受験生にもぜひ購入して貰いたいシリーズ本です。
個人的には春期講習も一段落して一息・・・・というところですか。
先日までの寒の戻りから一転して、昨日は暖かい一日でした。
さて、
「知は力なり(Ipsa scientia potestas est)」となりと言いますが、まさに記述問題では知識の差が如実に得点差として表れます。
C3J添削課題4の問題(c)
「塩酸をNaOHで中和滴定した時に使用するpH指示薬」と
「酢酸をNaOHで滴定した時に使用するpH指示薬」の選定に関する記述
では、指示薬の変色域とpHジャンプ(pH飛躍)の関係がポイントになります。
指示薬(HInで表す)自身も、弱い酸または塩基で、
(酸性の色)HIn ⇄ H+ + In-(アルカリ性の色)
の平衡が存在し、色の変化が肉眼で認められる範囲は指示薬の色調によって異なりますが、
おおよそ 10 > (酸性色の濃さ)÷(アルカリ性色の濃さ) > 0.1 とされ、
酸型とアルカリ型を示すpHの間隔はおよそ2となります。
その間では、酸性型とアルカリ性型の濃度の比に応じた中間色を示します。
この中間色の範囲が変色域で、その中心はpKHInです。
pHが1の強酸10mLをpH13の強塩基で滴定した場合、

のような滴定曲線となります。
この滴定曲線の中で、中和点の前後で急激にpHが変化している部分がpHジャンプ(pH飛躍)です。pH指示薬は、その変色域がpH飛躍(pHジャンプ)の範囲内にあるものを選択する必要があります。
pHジャンプ(pH飛躍)が起こる理由は、
pH(水素イオン指数)が対数だからです。
下図に明らかなように、当量点に近づくほど、単位滴下量あたりのpHの変化が大きくなります。

0.10mol/Lの塩酸10mLを0.10mol/LのNaOH水溶液で中和滴定すると、約8.2mL滴下したところで濃度が10分の1の0.010mol/Lになりますが、その10分の1の0.001mol/Lにするには1.6mLの滴下でよく、さらにその10分の1にするには0.18mLの追加で済みます。
このように、pHが1変化するのに要するNaOH水溶液の滴下量は、当量点(中和点)に近づくほど小さくなるため、滴定曲線の傾きは中和点でほぼ垂直(無限大)になるのです。
定量分析の実験手順と注意点,操作の意味は、
図解とフローチャートによる定量分析(技報堂出版) にフローチャート付きで詳しく記載されています。東大で頻出の実験に関する記述対策として、受験生にもぜひ購入して貰いたいシリーズ本です。
水素化合物の沸点 [C3J-東大化学 日記]
こんにちは~ (*^_^*)/
暖かくなったと思ったら、ここのところ冷えますねぇ。
春期講習も半ばなのに、マフラーが手放せません。
さて、今回は分子間結合について
入試では、
分子間結合は分子間力と水素結合とに分けて考えます。
分子間力(intermolecular force)は、
・交換斥力=かなり近距離においてのみ有効なパウリの排他原理に由来する反発力
ある程度以上近づくと電子雲の重なりが生じ、電子の交換相互作用が起こる事によって
生じる力です。距離が遠くなると急激に減少するので、入試では考えなくとも良いです。
・ファンデルワールス力,電荷移動力=比較的遠距離に於いても有効な引力
① 電荷移動力=電子供与体Dと電子受容体Aとの間に働く引力
非結合構造D・・・A と 電荷移動構造D+・・・A- との間の共鳴による安定化に相当
大学入試では考えなくて良いです。
② ファンデルワールス力=全ての分子間に働く分散力と有極性分子間に働く配向力と誘起力
からなる引力
に大別されます(化学辞典/森北出版)。
入試では、
分子間力≒ファンデルワールス力と考えて良いでしょう。
水素結合は、入試問題でも記述がよく出題されますね。
水素結合の説明は聖マリの解答例として記載していますので、その大問3の[6]を参照して下さい。
さて、
入試で頻出の問題の一つに
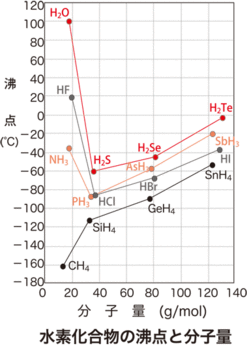
を説明させる記述問題があります。
分子間結合が強いほど、結合を切るのに多くのエネルギーが必要な為、沸点は高くなります。
14族の水素化合物は、正四面体構造なので、結合の極性モーメントはの合計はゼロ(正電荷の重心と負電荷の重心が一致するため互いに打ち消し合う)なので、完全な無極性分子です。
分子間力(ファンデルワールス力)は、分子が大きいほど強くなるため、分子量が大きいほど沸点が高くなります。
それに対して、
15,16,17族の水素化合物は、極性分子なので水素結合しており、その分だけ14族の水素化合物に比べて沸点が高くなっています。
この関係は、有機化学では、同じ分子量の炭化水素に対するアルコールやカルボン酸の沸点が高いのと同じです。
15,16,17族の水素化合物の中でも、水H2O,フッ化水素HF,アンモニアNH3は、
分子量に比べて「異常に高い沸点」です。
それは、酸素O,フッ素F,窒素Nの電気陰性度が大きいため、
他の水素化合物に比べて分子の極性がきわめて大きく、
・極性 = 電気陰性度の差が大きいほど電荷の偏りが大きくなり
極性が大きくなる。
分子間に働く水素結合が著しく強くなっている
・水素結合 = クーロン力(静電気力)は電荷の積に比例するので
極性が大きいほど水素結合は強くなる
からです。
記述の場合に重要なのは、
「他の水素化合物も水素結合しているが、それに比べて著しく強い水素結合をしている」
という旨を明記すべき事です。
よく
「水H2O,フッ化水素HF,アンモニアNH3は水素結合しているから沸点が高い」
という解答例を目にしますが、
前後の文脈によっては、「他の15,16,17族の水素化合物が水素結合していない(分子間力のみ)」
のようにしか読み取れないものもあり、それは明らかな間違いです。
注意して下さい。
暖かくなったと思ったら、ここのところ冷えますねぇ。
春期講習も半ばなのに、マフラーが手放せません。
さて、今回は分子間結合について
入試では、
分子間結合は分子間力と水素結合とに分けて考えます。
分子間力(intermolecular force)は、
・交換斥力=かなり近距離においてのみ有効なパウリの排他原理に由来する反発力
ある程度以上近づくと電子雲の重なりが生じ、電子の交換相互作用が起こる事によって
生じる力です。距離が遠くなると急激に減少するので、入試では考えなくとも良いです。
・ファンデルワールス力,電荷移動力=比較的遠距離に於いても有効な引力
① 電荷移動力=電子供与体Dと電子受容体Aとの間に働く引力
非結合構造D・・・A と 電荷移動構造D+・・・A- との間の共鳴による安定化に相当
大学入試では考えなくて良いです。
② ファンデルワールス力=全ての分子間に働く分散力と有極性分子間に働く配向力と誘起力
からなる引力
に大別されます(化学辞典/森北出版)。
入試では、
分子間力≒ファンデルワールス力と考えて良いでしょう。
水素結合は、入試問題でも記述がよく出題されますね。
水素結合の説明は聖マリの解答例として記載していますので、その大問3の[6]を参照して下さい。
さて、
入試で頻出の問題の一つに

を説明させる記述問題があります。
分子間結合が強いほど、結合を切るのに多くのエネルギーが必要な為、沸点は高くなります。
14族の水素化合物は、正四面体構造なので、結合の極性モーメントはの合計はゼロ(正電荷の重心と負電荷の重心が一致するため互いに打ち消し合う)なので、完全な無極性分子です。
分子間力(ファンデルワールス力)は、分子が大きいほど強くなるため、分子量が大きいほど沸点が高くなります。
それに対して、
15,16,17族の水素化合物は、極性分子なので水素結合しており、その分だけ14族の水素化合物に比べて沸点が高くなっています。
この関係は、有機化学では、同じ分子量の炭化水素に対するアルコールやカルボン酸の沸点が高いのと同じです。
15,16,17族の水素化合物の中でも、水H2O,フッ化水素HF,アンモニアNH3は、
分子量に比べて「異常に高い沸点」です。
それは、酸素O,フッ素F,窒素Nの電気陰性度が大きいため、
他の水素化合物に比べて分子の極性がきわめて大きく、
・極性 = 電気陰性度の差が大きいほど電荷の偏りが大きくなり
極性が大きくなる。
分子間に働く水素結合が著しく強くなっている
・水素結合 = クーロン力(静電気力)は電荷の積に比例するので
極性が大きいほど水素結合は強くなる
からです。
記述の場合に重要なのは、
「他の水素化合物も水素結合しているが、それに比べて著しく強い水素結合をしている」
という旨を明記すべき事です。
よく
「水H2O,フッ化水素HF,アンモニアNH3は水素結合しているから沸点が高い」
という解答例を目にしますが、
前後の文脈によっては、「他の15,16,17族の水素化合物が水素結合していない(分子間力のみ)」
のようにしか読み取れないものもあり、それは明らかな間違いです。
注意して下さい。
熱に関する用語の使い方 [C3J-東大化学 日記]
こんにちは~ (*^_^*)/
今回の添削課題で使い方の間違いが多かった用語 についてチェックしてみましょう。
・熱運動 = 熱エネルギーにより粒子がランダムに動くこと(熱振動とは似て非なる概念)
・対流 = 流体(気体や液体)において、温度差や溶質濃度などによって密度差が生じ、
上部の高密度な部分が重力によって引き下ろされて生じる流動現象
・拡散=流体(気体や液体)が熱運動によって自発的に散らばり広がっていく現象
・非晶質(アモルファス)=単位構造が繰り返す結晶構造を持たないが、局所的な秩序構造を持つ
もの
「規則性がない」という意味で「無定型」固体と呼ぶ場合もある。
・振動=同じ場所での物質の周期的な運動で、固体では粒子が相対位置を変えずに細かく
震えている。
あと、極性について
・極性=電気的な偏りのこと
ゆえに、「単原子イオンの極性」は変![[どんっ(衝撃)]](https://blog.ss-blog.jp/_images_e/161.gif)
今回の添削課題で使い方の間違いが多かった用語 についてチェックしてみましょう。
・熱運動 = 熱エネルギーにより粒子がランダムに動くこと(熱振動とは似て非なる概念)
・対流 = 流体(気体や液体)において、温度差や溶質濃度などによって密度差が生じ、
上部の高密度な部分が重力によって引き下ろされて生じる流動現象
・拡散=流体(気体や液体)が熱運動によって自発的に散らばり広がっていく現象
・非晶質(アモルファス)=単位構造が繰り返す結晶構造を持たないが、局所的な秩序構造を持つ
もの
「規則性がない」という意味で「無定型」固体と呼ぶ場合もある。
・振動=同じ場所での物質の周期的な運動で、固体では粒子が相対位置を変えずに細かく
震えている。
あと、極性について
・極性=電気的な偏りのこと
ゆえに、「単原子イオンの極性」は変
使われなくなった化学用語・単位 [C3J-東大化学 日記]
こんにちは~ (*^_^*)/
お馬鹿な政治家は国の災厄ですね┐(´ー`)┌
財源の裏付けのない子ども手当
しかも国外在住の日本国民(在外邦人)には支給されないで、日本在住の外国人には支給されるとか・・・( ̄○ ̄;)
さすが、何億円も子ども手当を受け取っていながら、発覚しなければ贈与税を払わなかった「友愛」首相の考える政策はひと味違いますね。![[むかっ(怒り)]](https://blog.ss-blog.jp/_images_e/152.gif)
票の入らない在外邦人より、「外国人参政権」付与で票になる外国人の方が大事なんですね。
さて、政治家やマスコミは文系出身の方が大半なので、科学技術について無知な場合が多く、そのために産業界ひいては国民生活が悪影響を受ける場合があります。パフォーマンス優先の事業仕分けがまさにそれ。
資源もなく食糧の自給さえできない日本が、科学技術でトップに立っていなくて、どうやってものを輸入できるのでしょうか?
さて、
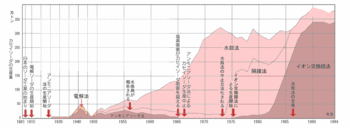
「水銀電解法」をご存じでしょうか?
食塩水を電気分解して苛性ソーダを生産する工業的製法の一つで、現在でも世界的には広く使用されていますが、日本では0%です。
著者が不勉強な参考書や問題集の中には、「水銀電解法」が「水俣病の水銀中毒」の原因であったかのような記述が散見されますが、事実誤認による誤りです(1973年5月に大牟田で第三水俣病発生の報道がありましたが、7月に九州大学医学部により否定されています)。
その経緯については、徳島大学の名誉教授・岡崎達也氏が、化学1993年7月号(化学同人)に、「水銀法消滅とその背景」とのタイトルで寄稿した論文に詳細に記されています。
世界全体では現在でも水銀法を多用しているのに、日本では0%です。
日本の水銀法はクローズドシステム化が完成されつつありましたが、1 9 5 3 年末から発生した水俣病を受けて水銀法の廃止が決定し、稼働中の水銀法工場を廃棄し、技術的に劣るアスベスト隔膜法の工場を建設するという世界でもまれな対策が取られました。
1 9 8 6 年6 月に全ての逆行転換を終えましたが、これにより10年の歳月と4000億円以上の投資を無駄にしたといわれています。
もちろん、余分にかかったコストは製品単価に上積みされて、国民が最終的に負担する事になります。
[参考]
・水俣病 = チッソ水俣工場のアセチレン水和反応の反応塔で副生した微量の塩化メチル水銀が工場排水中に混入し、水域の魚介類に蓄積され、それを反復経口摂取した付近の住民に有機水銀中毒を起こさせたとされる。
・塩化メチル水銀(CH3HgCl) = 硫黄(S)基と結合しやすく、メチオニンやシステインの硫黄(S)基に結合して蛋白質の立体構造を変え、神経細胞を変性・壊死させると考えられる。
ちなみに、
初歩的な化学や物理の知識があれば「怪しい(・_・)エッ....?」と思うこんなもの(YouTube)にさえ、政治家やマスコミはまんまと引っかかるんですね。
水で走る自動車(YouTube)が発表され、マスコミは疑念も挟まずに報道し、民主党・無所属ネット議員団のまちづくり部会長「中川隆弘」議員と環境農林部会長「森みどり」議員も出席してのお披露目までされていました。
∑( ̄口 ̄)
「理科の偏差値が50未満の政治家は、科学の話に口を挟んではいけない」という法律が必要ですよね。
政策を考える前に、まず勉強して下さい。(*´Д`)=з
国を動かす責任を負うのですから、被選挙権にも大学入試問題のような資格試験が必要なのでは?
お馬鹿な政治家は国の災厄ですね┐(´ー`)┌
財源の裏付けのない子ども手当
しかも国外在住の日本国民(在外邦人)には支給されないで、日本在住の外国人には支給されるとか・・・( ̄○ ̄;)
さすが、何億円も子ども手当を受け取っていながら、発覚しなければ贈与税を払わなかった「友愛」首相の考える政策はひと味違いますね。
票の入らない在外邦人より、「外国人参政権」付与で票になる外国人の方が大事なんですね。
さて、政治家やマスコミは文系出身の方が大半なので、科学技術について無知な場合が多く、そのために産業界ひいては国民生活が悪影響を受ける場合があります。パフォーマンス優先の事業仕分けがまさにそれ。
資源もなく食糧の自給さえできない日本が、科学技術でトップに立っていなくて、どうやってものを輸入できるのでしょうか?
さて、
「水銀電解法」をご存じでしょうか?
食塩水を電気分解して苛性ソーダを生産する工業的製法の一つで、現在でも世界的には広く使用されていますが、日本では0%です。
著者が不勉強な参考書や問題集の中には、「水銀電解法」が「水俣病の水銀中毒」の原因であったかのような記述が散見されますが、事実誤認による誤りです(1973年5月に大牟田で第三水俣病発生の報道がありましたが、7月に九州大学医学部により否定されています)。
その経緯については、徳島大学の名誉教授・岡崎達也氏が、化学1993年7月号(化学同人)に、「水銀法消滅とその背景」とのタイトルで寄稿した論文に詳細に記されています。
世界全体では現在でも水銀法を多用しているのに、日本では0%です。
日本の水銀法はクローズドシステム化が完成されつつありましたが、1 9 5 3 年末から発生した水俣病を受けて水銀法の廃止が決定し、稼働中の水銀法工場を廃棄し、技術的に劣るアスベスト隔膜法の工場を建設するという世界でもまれな対策が取られました。
1 9 8 6 年6 月に全ての逆行転換を終えましたが、これにより10年の歳月と4000億円以上の投資を無駄にしたといわれています。
もちろん、余分にかかったコストは製品単価に上積みされて、国民が最終的に負担する事になります。

[参考]
・水俣病 = チッソ水俣工場のアセチレン水和反応の反応塔で副生した微量の塩化メチル水銀が工場排水中に混入し、水域の魚介類に蓄積され、それを反復経口摂取した付近の住民に有機水銀中毒を起こさせたとされる。
・塩化メチル水銀(CH3HgCl) = 硫黄(S)基と結合しやすく、メチオニンやシステインの硫黄(S)基に結合して蛋白質の立体構造を変え、神経細胞を変性・壊死させると考えられる。
ちなみに、
初歩的な化学や物理の知識があれば「怪しい(・_・)エッ....?」と思うこんなもの(YouTube)にさえ、政治家やマスコミはまんまと引っかかるんですね。
水で走る自動車(YouTube)が発表され、マスコミは疑念も挟まずに報道し、民主党・無所属ネット議員団のまちづくり部会長「中川隆弘」議員と環境農林部会長「森みどり」議員も出席してのお披露目までされていました。
∑( ̄口 ̄)
「理科の偏差値が50未満の政治家は、科学の話に口を挟んではいけない」という法律が必要ですよね。
政策を考える前に、まず勉強して下さい。(*´Д`)=з
国を動かす責任を負うのですから、被選挙権にも大学入試問題のような資格試験が必要なのでは?
使われなくなった化学用語・単位 [C3J-東大化学 日記]
こんにちは~ (*^_^*)/
使わなくなったもの、第2段です。
個人的に使わなくなったものと言えば、
Made in Chinaの食品ですね。大陸の環境破壊(YouTube)は、黄砂によって九州が被害を受けるくらいですから、半端ではありません。食品の安全性なんぞ、期待する方が無駄というものです。マスコミは最近報道しなくなりました(YouTube)が・・・・
「むき栗」は好きですが、大陸(YouTube)産はちょっと怖い(YouTube)ので、最近食べてないですね![[もうやだ~(悲しい顔)]](https://blog.ss-blog.jp/_images_e/143.gif)
さて、今回の使われなくなった用語は、有機化合物です。
・沼気(しょうき) = メタン CH4
・木精(もくせい) = メタノール CH3OH
・酒精(しゅせい) = エタノール C2H5OH
・糊精(こせい) = デキストリン
・含水炭素(がんすいたんそ) = 炭水化物(糖類)
・酒石(しゅせき) = 酒石酸水素カリウム
・吐酒石(としゅせき) = 酒石酸アンチモニルカリウム
・焦性葡萄酸(しょうせいぶどうさん) = ピルビン酸
※ 「焦性」とは、「元の酸を強熱したり乾留した時にできる」という意味です。
・薄荷脳(はっかのう) = メントール
・満那(まんな) = マンニトール
・油酸(ゆさん) = オレイン酸 C17H33COOH
・繊維素(せんいそ) = セルロース
「繊維素」は、生物学ではフィブリンを指します。
・竜脳(りゅうのう) = ボルネオール
・・・・など、探せば結構あるものですね。
まだ、社会的には抹殺されていないものの、高校教科書からは排除されつつある用語もあります。
・葡萄糖(ぶどうとう) = グルコース C6H12O6
・果糖(かとう) = フルクトースC6H12O6
・脳糖(のうとう) = ガラクトース C6H12O6
・麦芽糖(ばくがとう) = マルトース C12H22O11
・蔗糖(しょとう) = スクロース,サッカロース C12H22O11
・乳糖(にゅうとう) = ラクトース C12H22O11
・樟脳(しょうのう) =カンファー C10H16O
・石蝋(せきろう) = パラフィン
※ パラフィン = 炭素数が20以上のアルカン (常温で固体)
・石炭酸(せきたんさん) = フェノール C6H5-OH
単糖類,二糖類の名称などは、そのまま使い続けても良いと思いますが・・・・
小学校の交ぜ書きや常用漢字でも思いますが、ふりがな(ルビ)で英語名を表記すれば良いだけだと思いませんか?
大学入試では、こうした古い(?)表現を態(わざ)と使って表記することもあるので、知っておいて損はしないと思います。
昔の本などを読んでいると、しばしば目にする言葉も入っていますよね。
使わなくなったもの、第2段です。
個人的に使わなくなったものと言えば、
Made in Chinaの食品ですね。大陸の環境破壊(YouTube)は、黄砂によって九州が被害を受けるくらいですから、半端ではありません。食品の安全性なんぞ、期待する方が無駄というものです。マスコミは最近報道しなくなりました(YouTube)が・・・・
「むき栗」は好きですが、大陸(YouTube)産はちょっと怖い(YouTube)ので、最近食べてないですね
さて、今回の使われなくなった用語は、有機化合物です。
・沼気(しょうき) = メタン CH4
・木精(もくせい) = メタノール CH3OH
・酒精(しゅせい) = エタノール C2H5OH
・糊精(こせい) = デキストリン
・含水炭素(がんすいたんそ) = 炭水化物(糖類)
・酒石(しゅせき) = 酒石酸水素カリウム
・吐酒石(としゅせき) = 酒石酸アンチモニルカリウム
・焦性葡萄酸(しょうせいぶどうさん) = ピルビン酸
※ 「焦性」とは、「元の酸を強熱したり乾留した時にできる」という意味です。
・薄荷脳(はっかのう) = メントール
・満那(まんな) = マンニトール
・油酸(ゆさん) = オレイン酸 C17H33COOH
・繊維素(せんいそ) = セルロース
「繊維素」は、生物学ではフィブリンを指します。
・竜脳(りゅうのう) = ボルネオール
・・・・など、探せば結構あるものですね。
まだ、社会的には抹殺されていないものの、高校教科書からは排除されつつある用語もあります。
・葡萄糖(ぶどうとう) = グルコース C6H12O6
・果糖(かとう) = フルクトースC6H12O6
・脳糖(のうとう) = ガラクトース C6H12O6
・麦芽糖(ばくがとう) = マルトース C12H22O11
・蔗糖(しょとう) = スクロース,サッカロース C12H22O11
・乳糖(にゅうとう) = ラクトース C12H22O11
・樟脳(しょうのう) =カンファー C10H16O
・石蝋(せきろう) = パラフィン
※ パラフィン = 炭素数が20以上のアルカン (常温で固体)
・石炭酸(せきたんさん) = フェノール C6H5-OH
単糖類,二糖類の名称などは、そのまま使い続けても良いと思いますが・・・・
小学校の交ぜ書きや常用漢字でも思いますが、ふりがな(ルビ)で英語名を表記すれば良いだけだと思いませんか?
大学入試では、こうした古い(?)表現を態(わざ)と使って表記することもあるので、知っておいて損はしないと思います。
昔の本などを読んでいると、しばしば目にする言葉も入っていますよね。
使われなくなった化学用語・単位 [C3J-東大化学 日記]
こんにちは~ (*^_^*)/
現在、化学の教科書から追放されていますが、工業界や一般用語として使われている化学用語や単位があります。
例えば、梧桐の愛車は、空気圧が「100 PSI / 6.9Bar Max」と記載されています。SI単位に直すと690kPaですが、使ってるポンプはatm表示になっていますから、限度圧6.80atmと換算し直す必要があります。
日本では、官庁からの号令で一斉に圧力はSI単位のPa表記へ変えました(電車や消防車の圧力計など)が、けっこう昔の単位(非SI単位)も広く使用されていて混在しているのが現状です。
医学部では、血圧計などに今でも水銀柱mmHgを使っていますしね。
昔から知られていた物質の固有名詞も、化学の教科書から抹殺されています。
そのため、化学屋が昔の物語の中に登場する物質名を分からなかったりしますね。
というわけで、化学の教科書から排除された物質名をまとめてみました。
(消石灰や生石灰くらいはまだ残っていますが・・・)
・金剛石(こんごうせき) = ダイヤモンド C
・膽礬(たんばん) = 硫酸銅(Ⅱ)五水和物 CuSO4・5H2O
・緑礬(りょくばん) = 硫酸鉄(Ⅱ)七水和物 FeSO4・7H2O
・皓礬(こうばん) = 硫酸亜鉛七水和物 ZnSO4・7H2O
・赤礬(せきばん) = 硫酸コバルト七水和物 CoSO4・7H2O
・芒硝(ぼうしょう) = 硫酸ナトリウム十水和物 Na2SO4・10H2O
・瀉利塩(しゃりえん) = 硫酸マグネシウム MgSO4・7H2O
・甘汞(かんこう) = 塩化水銀(Ⅰ) Hg2Cl2
・昇汞(しょうこう) = 塩化水銀(Ⅱ) HgCl2
・黄降汞(おうこうこう) = 酸化水銀(Ⅱ) HgO
・白降汞(はっこうこう) = アミノ塩化第二水銀 Hg(NH2)Cl
※ 汞(こう) = 水銀Hgのこと
・赤血塩(せっけつえん) = ヘキサシアノ鉄(Ⅲ)酸カリウム K3[Fe(CN)6]・3H2O
・黄血塩(おうけつえん) = ヘキサシアノ鉄(Ⅱ)カリウム K4[Fe(CN)6]
・青酸(せいさん) = シアン化水素 HCN
・笑気(しょうき) = 一酸化二窒素(亜酸化窒素) N2O
・磠砂(ろしゃ)・塩安(えんあん) = 塩化アンモニウム NH4Cl
・密陀僧(みつだそう) = 酸化鉛(Ⅱ) PbO
・黄鉛 = クロム酸鉛(Ⅱ) PbCrO4
・鉛糖 = 酢酸鉛(Ⅱ) Pb(CH3COO)2
・光明丹(こうみょうたん)・鉛丹(えんたん) = 四三酸化鉛 Pb3O4
・亜鉛華 = 酸化亜鉛 ZnO
・苛性加里(かせいかり) = 水酸化カリウム KOH
・苛性曹達(かせいそうだ) = 水酸化ナトリウム NaOH
・加爾基(かるき) = さらし粉 CaCl(ClO)・H2O
・重曹(じゅうそう) = 炭酸水素ナトリウム NaHCO3
・硝石(しょうせき) = 硝酸カリウム KNO3
・消石灰( しょうせっかい) = 水酸化カルシウム Ca(OH)2
・生石灰(せいせっかい) = 酸化カルシウム CaO
・石膏(せっこう) = 硫酸カルシウム二水和物 CaSO4・2H2O
・曹達灰(そうだばい) = 炭酸ナトリウム Na2CO3
・礬土(ばんど) = 酸化アルミニウム Al2O3
・硼砂(ほうしゃ) = 四ホウ酸ナトリウム十水和物Na2B4O5(OH)4・8H2O
またはNa2B4O7・10H2O
・沃剥(ようぽつ) = ヨウ化カリウム KI
・鹿角塩(ろっかくえん) = 炭酸アンモニウム (NH4)2CO3
・燐安(りんあん) = リン酸アンモニウム (NH4)3PO4
・雷汞(らいこう) = 雷酸水銀 Hg(ONC)2
元素名では
・水鉛 = モリブデン Mo
・蒼鉛 = ビスマス Bi
・ニオビウム = ニオブ Nb
・曹達(そうだ) = ナトリウム Na
現在、化学の教科書から追放されていますが、工業界や一般用語として使われている化学用語や単位があります。
例えば、梧桐の愛車は、空気圧が「100 PSI / 6.9Bar Max」と記載されています。SI単位に直すと690kPaですが、使ってるポンプはatm表示になっていますから、限度圧6.80atmと換算し直す必要があります。
日本では、官庁からの号令で一斉に圧力はSI単位のPa表記へ変えました(電車や消防車の圧力計など)が、けっこう昔の単位(非SI単位)も広く使用されていて混在しているのが現状です。
医学部では、血圧計などに今でも水銀柱mmHgを使っていますしね。
昔から知られていた物質の固有名詞も、化学の教科書から抹殺されています。
そのため、化学屋が昔の物語の中に登場する物質名を分からなかったりしますね。
というわけで、化学の教科書から排除された物質名をまとめてみました。
(消石灰や生石灰くらいはまだ残っていますが・・・)
・金剛石(こんごうせき) = ダイヤモンド C
・膽礬(たんばん) = 硫酸銅(Ⅱ)五水和物 CuSO4・5H2O
・緑礬(りょくばん) = 硫酸鉄(Ⅱ)七水和物 FeSO4・7H2O
・皓礬(こうばん) = 硫酸亜鉛七水和物 ZnSO4・7H2O
・赤礬(せきばん) = 硫酸コバルト七水和物 CoSO4・7H2O
・芒硝(ぼうしょう) = 硫酸ナトリウム十水和物 Na2SO4・10H2O
・瀉利塩(しゃりえん) = 硫酸マグネシウム MgSO4・7H2O
・甘汞(かんこう) = 塩化水銀(Ⅰ) Hg2Cl2
・昇汞(しょうこう) = 塩化水銀(Ⅱ) HgCl2
・黄降汞(おうこうこう) = 酸化水銀(Ⅱ) HgO
・白降汞(はっこうこう) = アミノ塩化第二水銀 Hg(NH2)Cl
※ 汞(こう) = 水銀Hgのこと
・赤血塩(せっけつえん) = ヘキサシアノ鉄(Ⅲ)酸カリウム K3[Fe(CN)6]・3H2O
・黄血塩(おうけつえん) = ヘキサシアノ鉄(Ⅱ)カリウム K4[Fe(CN)6]
・青酸(せいさん) = シアン化水素 HCN
・笑気(しょうき) = 一酸化二窒素(亜酸化窒素) N2O
・磠砂(ろしゃ)・塩安(えんあん) = 塩化アンモニウム NH4Cl
・密陀僧(みつだそう) = 酸化鉛(Ⅱ) PbO
・黄鉛 = クロム酸鉛(Ⅱ) PbCrO4
・鉛糖 = 酢酸鉛(Ⅱ) Pb(CH3COO)2
・光明丹(こうみょうたん)・鉛丹(えんたん) = 四三酸化鉛 Pb3O4
・亜鉛華 = 酸化亜鉛 ZnO
・苛性加里(かせいかり) = 水酸化カリウム KOH
・苛性曹達(かせいそうだ) = 水酸化ナトリウム NaOH
・加爾基(かるき) = さらし粉 CaCl(ClO)・H2O
・重曹(じゅうそう) = 炭酸水素ナトリウム NaHCO3
・硝石(しょうせき) = 硝酸カリウム KNO3
・消石灰( しょうせっかい) = 水酸化カルシウム Ca(OH)2
・生石灰(せいせっかい) = 酸化カルシウム CaO
・石膏(せっこう) = 硫酸カルシウム二水和物 CaSO4・2H2O
・曹達灰(そうだばい) = 炭酸ナトリウム Na2CO3
・礬土(ばんど) = 酸化アルミニウム Al2O3
・硼砂(ほうしゃ) = 四ホウ酸ナトリウム十水和物Na2B4O5(OH)4・8H2O
またはNa2B4O7・10H2O
・沃剥(ようぽつ) = ヨウ化カリウム KI
・鹿角塩(ろっかくえん) = 炭酸アンモニウム (NH4)2CO3
・燐安(りんあん) = リン酸アンモニウム (NH4)3PO4
・雷汞(らいこう) = 雷酸水銀 Hg(ONC)2
元素名では
・水鉛 = モリブデン Mo
・蒼鉛 = ビスマス Bi
・ニオビウム = ニオブ Nb
・曹達(そうだ) = ナトリウム Na




